KEA managemnetではISO 22716に関連した各種サポートを実施しております
認証取得検討の際は是非お問い合わせください。
現場運用と費用対効果に合わせたシステム構築、内部監査、教育訓練、委託先評価などのISO 22716に関するサポートを提供しております。関連記事はこちらから
ISO22716(化粧品GMP)の認証について
2007年に発行されたISO 22716は、日本化粧品工業会の自主基準に変わる新たな化粧品GMPとして運用が続けられております。従来は自主運用をベースに行われてきた活動ですが、近年はこのISO規格について認証を受ける企業/組織様も出てまいりました。私共にもISO22716認証に関して、どのように考えれば良いかのお問い合わせが増えてきております。
ISO22716の認証システムはISO 9001等の認証とは位置づけが全く異なります。お問い合わせの多くは、認証そのものの混同して捉えられている誤解からきているため本ページにまとめさせていただきました。
専門用語を少なくして出来る限り解りやすくまとめました。ISO22716取得を目指している企業/組織様へのご参考になれば幸いです。
ISOの認定/認証システムとは(特に品質マネジメントシステム関連領域)
下記に認証システムの概略図を示します。認定/認証には異なる3つの組織が登場します。特に認定機関と認証機関を混同しないように注意してください。
A:認定機関(認定に責任を持つ組織です、各国に1つor2つあります)
B:認証機関(実際に監査に来る方が所属している組織です、国内系/外資系と多くの組織があります)
C:取得組織(自分の会社です)
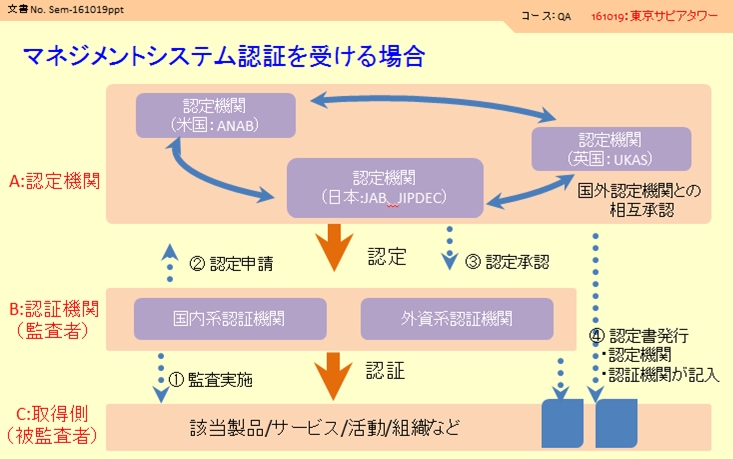
実際の認証プロセスを追ってみましょう。
①:認証機関があなたの会社に監査に来ます。
②:監査結果は認証機関がまとめ→認定機関へ申請を行います。
(この申請部分は、あなたの会社側からは見えません)
③:問題がなければ認定機関により了承が行われます。
④:正式に認証され、適合マークが利用可能になります。
認証に関して表面上は①+④、B:認証機関、C:取得組織のやり取りで完了します。
実際は、A:認定機関から認定を受けたB:認証機関が代理で監査を行い、その結果を認定機関へ報告。A:認定機関が認定を発行するというプロセスになっています。これにより高い客観性と品質を保っています。
つまり、実際に監査に来る監査者は、認定機関から依頼を受けてあなたの会社に来ているとの位置づけです。
このため認証マークには「監査した機関」「認定を出した機関」の2つが並列して記載されます。
 マーク例は、
マーク例は、
認証機関(監査を実施した機関):JQA
認定機関(認定を出した機関):JAB
各国にある認定機関は、国際相互承認という形でその品質を担保しています。
ISO 22716認証プロセス
それではISO 22716認証とはどのようなステップで進むのでしょうか?
ここでは上記とは異なり2つの組織しか登場しません。
B:認証機関(実際に監査に来る方が所属している組織です、国内系/外資系と多くの組織があります)
C:取得組織(自分の会社です)
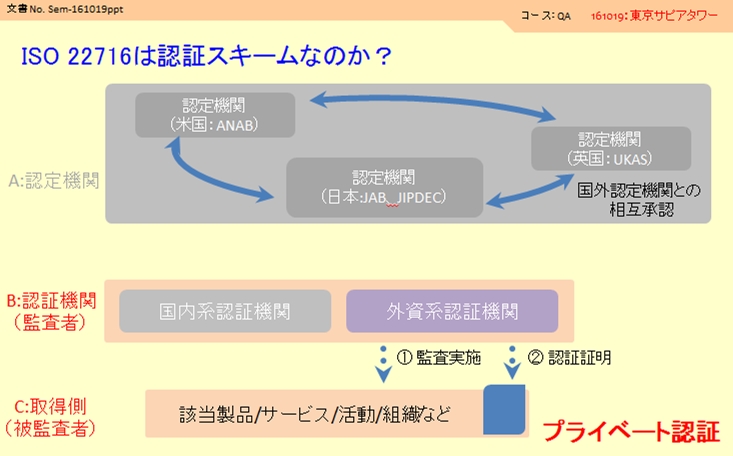
実際の認証プロセスを追ってみましょう。
①:認証機関があなたの会社に監査に来ます。
②:問題がなければ認証機関が自主的に承認して、認証発行を行います。
ISO 22716認証には国単位で登録されている認定機関の存在はなく、監査機関が自主的にOKを出す仕組みになっています。このような認証を「プライベート認証」といいます。
(品質マネジメントシステム時のような二段階の認証システムではないため、既に認証済みの企業様のマークを確認すると、認証機関のみの表示になっていることがお分かりになるかと思います)
認定機関を介さず自主的に認証を出すプロセスは、高い客観性が望まれる「第三者監査」に好ましくないと表現される場合があります。(自分で採点して、合格通知を出し、さらに対価として金額を請求できるため)
ISO 17021:適合性評価-マネジメントシステムの審査及び認証 を行う機関に対する要求事項では、監査者が依頼者との利害関係を持つことを禁止しています。
お問い合わせの中には、ISO 9001等の品質マネジメントシステム認証とISO22716認証を「同等」と誤解されている方がいらっしゃいます。プライベート認証は、あくまでも適合の自己宣言を補助する位置づけと考えると適切です。
ISO 22716認証を受けるために注意が必要な事
現在、ISO22716に関してプライベート認証を行っている機関がいくつかあります。
上記まとめの通り認定機関を介さない監査/認証システムのため、自社が目指すべき方向性…
「自社組織に対する22716認証の目的は何であるか」
「どのような活動プロセスを継続していくか」
「そのための自社内課題は」
などを事前に明確に設定することが必要です。
認証監査は規格との適合性のみを見て実行されるため、取得だけであれば比較的容易です。
(特に外資系の認証機関はJAB:日本適合性認定協会で禁止している予備監査を実施しており、先に答え合わせが出来てしまう)
「取得後に、自社にとってどのような価値ある活動へと変換していくか」
「それが具体的成果につながるか」
の点については、取得とは別軸で考えていかなければなりません。
認証がゴールではなく、その後の活動レビューで成果を共有していくことが目的地と認識することが適切であると考えます。
このため、証機関を選定する際は、目的地を具体的に共有/そのポイントを監査時に抽出/進捗を追うことが可能、等の要素を重点としてください。
ISO22716は2007年度版発行の古い規格になりました。現行のISO9001:2015は、文書体系構築と品質保証を主目的としていた旧版から、マネジメントシステムを主眼とした内容に変遷しています。特に上記のような課題設定について、トップマネジメントを含めた責任が明確に設定されています。
ISO 22716承認を目指す企業様において現在9001を運用されている場合、2015年度版の良点を組み込み活動推進することがポイントになると考えます。
キアマネジメントではISO 22716を元にした品質マネジメントシステム推進活動をサポートしております
化粧品GMPを基礎から学びたい、認証を検討しているが手の付け所が解らない
現システムの妥当性を確認したい、内部監査システムを強化したい、取引先の品質を担保したい
などのご要望にお応えいたします。詳細はメール/お問い合わせフォームよりご連絡下さい

